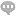超声微泡造影剂在******中应用。***的**早指标之一是单核细胞与内皮细胞的***和附着。这是由白细胞粘附分子(lam)如细胞间粘附分子-1(ICAM-1)的上调介导的。1997年,用于常规心肌超声造影的带有白蛋白壳的超声造影剂在某些病理条件下通过心肌的转运时间较慢。在体外实验中,这些微泡优先粘附在表达lam的内皮细胞上。随后,含有针对ICAM-1的单克隆抗体的超声造影剂在体外和体内均显示出良好的结合效率。Villanueva等人和其他人描述了使用微泡对炎症进行主动靶向,其中在炎症反应期间***的内皮细胞使用微泡进行靶向。Takalkar等人使用平行板流室来测定抗icam-1靶向的微泡对白细胞介素-1人工***的内皮细胞的粘附性。增加了40倍与非靶向对照相比,靶向微泡发生了微泡粘附。微泡以高达100s-1的剪切速率粘附,这是较大小静脉的特征。其他白细胞粘附分子在炎症和缺血-再灌注损伤中上调。特别有趣的是p-选择素,它已被超声造影剂靶向炎症小鼠模型。Rychak等人**近证明了可变形微泡与p-选择素的靶向粘附。南京星叶生物研发的超声微泡造影剂是有脂质外壳包裹全氟丙烷惰性气体组成,平均尺寸约为500-700nm。天津超声微泡企业

微泡表面选择合适的偶联化学和修饰顺序取决于配体的类型。一个重要的考虑因素是配体的大小及其对生物利用度的影响。小的亲水分子,如代谢物和肽,可以直接偶联到聚合物间隔物上,而不会***影响聚合物动力学。相比之下,大的蛋白质配体,如抗体,由于剪切应力和涉及微泡分散的有机溶剂,容易变性。因此,抗体(~120 kDa)通常通过生物素-亲和素连接连接到预形成的微泡表面。所得到的复合物更像一个刚性支架,而不是一个自由的聚合物链(50),配体与聚合物刷(~5 kDa)被大块的亲和素分子(~60 kDa)很好地分离。江苏载药超声微泡荧光标记的靶向微泡在血管生成过程中的应用。
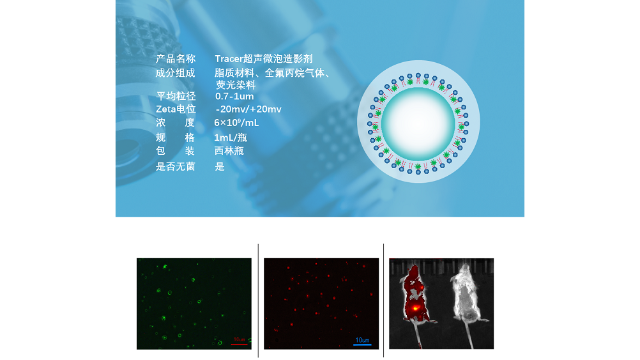
超声微泡的大小差异影响超声微泡的药代动力学、病变部位靶向、内吞过程和细胞摄取。人体生物系统对不同颗粒的反应不同,小于8µm的气泡具有模拟红细胞循环的优点,从而促进其扩散到血管和***间的循环中。除此之外,气泡的大小不应超过8µm,因为它可能导致并发症,如血流中的动脉栓塞。因此,超声微泡在早期开发时就被用作理想的造影剂,并被应用于超声分子成像、磁共振成像(MRI)、近红外成像(NIRF)、磁共振成像(MRI)、正电子发射断层扫描(PET)、单光子发射计算机断层扫描(SPECT)、光学成像和对比增强超声(CEUS)成像的诊断。目前,超声微泡被用作***和***药物、抗体、基因和miRNA的递送剂,它们可以与光敏剂结合以辅助成像。超声微泡还可以通过MRI/NIR/ US等三模成像方法提高***效率,从而减少重复,对靶***/组织的危害相对较小。
超声溶栓是一种用于溶解***引起的血管血栓(血栓)的***方法。***过程是利用MNB造影剂与超声联合产生空化效应,以破坏纤维蛋白网。Ling等人利用EDC/NHS偶联cRGD肽,利用溶剂乳液蒸发法制备了环arg - gys - asp (cRGD)靶向PLGA MBs和纳米微泡,用于活性靶向血小板糖蛋白(GP) IIb/IIIa。cRGD靶向的MBs和纳米微泡的粒径/共轭比分别约为3µm/92.2%和220 nm/94.6%。为了模拟人体血液循环中的血栓栓塞,本研究采用兔血块结合频率为1.3 MHz的超声***的闭环血流装置。与其他***方法相比,cRGD靶向的纳米微泡在30分钟内表现出明显的凝血溶解,cRGD肽可有效结合血小板受体。153此外,超声频率可根据***目的进行调整。如:20 kHz ~ 1 MHz可有效溶栓,15427 ~ 200 kHz可促进动物溶栓,<1 MHz可促进血脑屏障打开。超声微泡的大小差异影响超声微泡的药代动力学、病变部位靶向、内吞过程和细胞摄取。

微泡空化时细胞膜和血管通透性的变化。电子显微镜已经证明,在细胞膜内产生的小孔与微泡的崩溃和射流的产生有关。根据超声参数,细胞膜内产生的孔隙可能是短暂的,导致细胞死亡或成功地将外源物质引入细胞质。除了改变细胞膜通透性外,将超声应用于含有微泡的小血管还能改变血管壁的通透性,导致颗粒外渗到间隙。这种***通透性的变化取决于泡的大小、壳的组成以及***直径与泡直径的比值。改变超声参数,如声压和脉冲间隔,以及物理参数,如注射部位和微血管压力,可以比较大限度地提高微球的局部药物递送。在超声中心频率为1MHz的情况下,0.75MPa的压力足以在体外大鼠肌肉微循环中产生***破裂。超声脉冲间隔既影响观察到外渗的点数,也影响输送的物质体积,两者在脉冲间隔为5s时均达到比较大值。人们认为,要使输送的物质体积比较大化,需要将微泡补充到脉冲之间的区域。研究还表明,随着***血压的升高,微泡通过***壁的运输也会增加。超声联合纳米微泡递送RNA。天津超声微泡企业
纳米微泡的直径通常在150-500纳米之间,是药物分布的诱人场景并且与微泡相比已证明可以改善聚集和保留。天津超声微泡企业
**初的微泡靶向实验是在静态条件下进行的:将气泡与目标表面接触(通常是倒置),在没有流动的情况下孵育几分钟,然后将剩余的自由气泡洗掉,测量保留气泡的数量和声学响应。然而,这种情况并不是脉管系统内真正靶向的良好模型,在脉管系统内,结合发生时没有任何流动停止。取决于配体-受体结合和脱离动力学,以及配体和受体的表面密度、血流和壁剪切条件,与靶标的结合可能发生,也可能不发生。结合可能是短暂的(几分之一秒),也可能是长久的(几秒或几分钟),这取决于在初始接触期间有多少牢固的键有机会形成。了解微泡靶向性的比较好方法是在体外受控条件下,以已知的流速、配体和受体密度进行靶向性研究。平行板流室通常用于这些研究。一些配体(如抗体)能够与目标抗原牢固结合(一旦结合发生解离抗体和抗原可能需要几天的时间,但这种结合并不总是很快的。在流动的情况下,颗粒上的配体与受体结合的时间非常有限。在极端情况下(大血管中1米/秒的血流),典型的配体与受体结合位点线性尺寸为1纳米时,必须在1纳秒内发生有效结合,这是一个极短的时间,与大多数抗体-抗原kon动力学常数不相容。天津超声微泡企业
文章来源地址: http://yyby.chanpin818.com/swzp/qtswzp/deta_24258618.html
免责声明: 本页面所展现的信息及其他相关推荐信息,均来源于其对应的用户,本网对此不承担任何保证责任。如涉及作品内容、 版权和其他问题,请及时与本网联系,我们将核实后进行删除,本网站对此声明具有最终解释权。



 [VIP第1年] 指数:3
[VIP第1年] 指数:3